|
|
|||
| Izotopy - to atomy, które
posiadają tę samą liczbę protonów, ale różnią się liczbą neutronów.
Izotopy różnią się masą atomową, ale należą do jednego pierwiastka i mają
niemal identyczne własności chemiczne.Ze względu na różnicę mas atomowych
izotopy mają jednak różne niektóre własności fizyczne, przy czym różnice
te są tym większe im większy jest rozrzut ich mas względem siebie. Różnice
w masach atomowych izotopów powodują, że w formie czystej mają one inną
gęstość, temperaturę wrzenia, topnienia i sublimacji. Różnice te
rozciągają się także na związki chemiczne o różnym składzie izotopowym. Izotopy promieniotwórcze zwane też krócej radioizotopami to niestabilne, radioaktywne izotopy, których atomy samoistnie rozpadają się, dając w wyniku inne atomy, cząstki elementarne oraz wydzielając energię w postaci promieniowania gamma. Izotopy promieniotwórcze charakteryzuje okres połowicznego zaniku, tj. czas w którym zanika połowa jąder danego pierwiastka. Okres połowicznego zaniku nie zależy od powiązań chemicznych atomu izotopu. Izotopy dzielą się na:
Występowanie izotopów komplikuje nieco obliczenia chemiczne (zobacz: stechiometria), powodując, że masy atomowe i co za tym idzie masy cząsteczkowe nie są liczbami całkowitymi, lecz liczbami z ułamkiem. Izotopy nie mają oddzielnych nazw z wyjątkiem izotopów wodoru, oznacza się je symbolem pierwiastka chemicznego z liczbą masową u góry po lewej stronie, np. 208Pb |
|
||
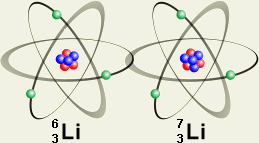
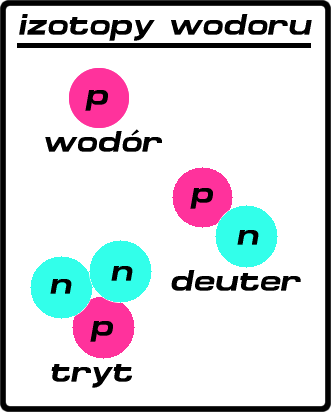
Pierwiastki mają po
kilka, a nawet kilkanaście izotopów. Np. wodór ma trzy izotopy:
|
|||
 Izotopy
Izotopy